运动医学新突破:外泌体“快递”miRNA,韧带重建愈合加速!
你是否曾因前交叉韧带(ACL)损伤而接受重建手术,却苦于术后恢复缓慢?传统的ACL重建手术虽能恢复膝关节稳定性,但术后肌腱与骨骼的愈合质量不高、愈合时间漫长,一直是困扰患者和医生的难题。近日,一项发表于国际权威期刊的研究为解决这一难题带来了新的希望。
背景:ACL重建的困境与希望
前交叉韧带损伤是常见的运动损伤,重建手术是治疗完全断裂的主要方法。然而,术后肌腱与骨之间的愈合过程往往需要数月时间,且愈合质量不尽如人意,导致患者重返运动的时间延长,再损伤风险增高。
近年来,骨髓基质细胞外泌体(BMSC-Exos)作为组织修复的新星备受关注。外泌体是细胞分泌的纳米级囊泡,能够携带蛋白质、RNA等生物活性物质,在细胞间通讯中扮演重要角色。然而,BMSC-Exos是否能促进ACL重建术后肌腱骨愈合,其具体机制又如何,尚不明确。
创新研究:外泌体中的miRNA是关键
研究发现BMSC-Exos通过其中富含的miR-23a-3p促进巨噬细胞从M1型向M2型极化,从而减轻早期炎症反应,加速ACL重建后的愈合过程。研究人员通过生物信息学分析发现,miR-23a-3p在大鼠BMSC-Exos中高表达,并且可以靶向干扰素调节因子1(IRF1)——M1巨噬细胞极化的关键调控因子。
机制揭秘:巨噬细胞极化的“开关”
巨噬细胞是免疫系统的重要成员,在不同微环境刺激下可极化为不同表型:M1型(促炎型)和M2型(抗炎型/修复型)。在组织损伤初期,M1型巨噬细胞主导炎症反应,清除坏死组织;随后M2型巨噬细胞逐渐增多,促进组织修复和再生。两者平衡对组织愈合至关重要。
本研究显示,BMSC-Exos中富含的miR-23a-3p能够靶向抑制IRF1表达,而IRF1是M1巨噬细胞极化的关键调控因子。这样一来,巨噬细胞极化平衡就向M2型倾斜,从而减轻炎症反应,促进组织修复。
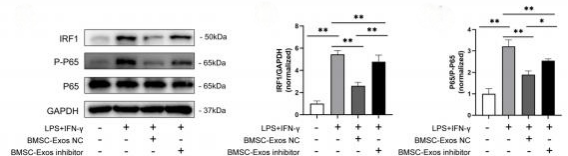
在体内实验中,研究人员建立了大鼠ACL重建模型,并将实验动物分为三组:
对照组,BMSC-Exos组,miR-23a-3p过表达BMSC-Exos组
结果发现:术后2周,miR-23a-3p过表达BMSC-Exos组局部M2巨噬细胞数量显著增加;术后4周和8周,该组大鼠表现出:
胫骨和股骨侧的骨隧道明显变小;移植物与骨组织界面变窄;骨体积/总体积比(BV/TV)升高;II型胶原α1水平上升;机械强度增强
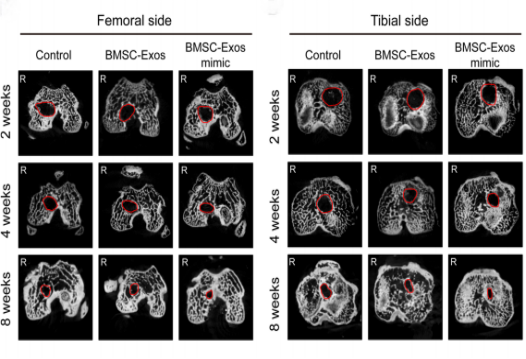
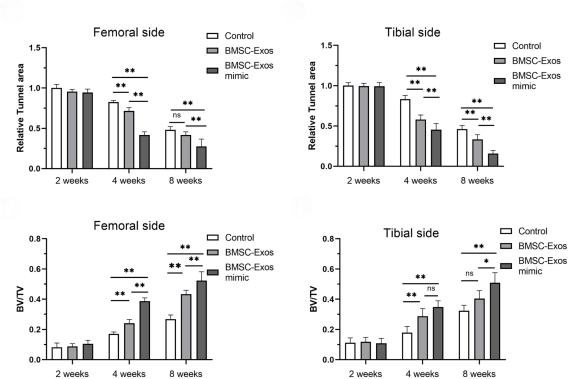
这些结果充分表明,miR-23a-3p过表达的BMSC-Exos能够显著促进ACL重建后的肌腱骨愈合过程。
临床意义:运动医学新前景
这项研究具有重要的临床意义:
1.提高愈合质量:通过促进肌腱骨愈合,可能降低移植物的失效风险,提高手术成功率。
2.缩短康复时间:加速愈合过程意味着患者可以更早开始康复训练,更快重返运动场。
3.提供新治疗策略:基于BMSC-Exos的治疗方法可能成为促进组织修复的无细胞治疗新策略,避免细胞治疗的某些风险。
4.精准调控免疫微环境:通过调控巨噬细胞极化,为实现免疫微环境的精准调控提供新思路。
展望未来
尽管这项研究是在大鼠模型中进行的,但它为临床治疗提供了新方向。未来研究可进一步探索:大型动物实验中是否也能观察到类似效果;最佳给药途径和剂量;长期安全性和有效性
;是否适用于其他类型的组织修复
随着进一步研究的深入,基于外泌体的治疗策略有望成为运动医学领域的新突破,为ACL损伤患者带来福音。
这项研究不仅揭示了BMSC-Exos通过miR-23a-3p-IRF1轴调控巨噬细胞极化促进肌腱骨愈合的机制,也为开发促进ACL重建后愈合的治疗策略提供了新思路。未来,我们或许只需要在手术中局部应用工程化外泌体,就能显著加速愈合过程,帮助患者更快更好地重返运动生涯。
版权声明:本文仅为科普分享,不作为诊疗建议。如有相关疾病,请及时就医并根据专业医师意见进行治疗。
