用 CRISPR‑Cas 给耐药基因上“锁”:阻断细菌水平基因转移的最新突破
【开篇导读】
“超级细菌”正成为全球公共健康的隐形炸弹。抗生素使用越多,细菌越擅长通过质粒、噬菌体或转座子在不同菌株间“偷渡”耐药基因,这种过程被称为水平基因转移(Horizontal Gene Transfer,HGT)。假如我们能在细菌内部布置一把“剪刀”,一旦发现耐药基因就剪断、销毁,它们还能轻松共享武器吗?2025 年《Nature Scientific Reports》发表的一项工作给出了积极答案:研究者设计了靶向 8 种常见耐药基因的 CRISPR‑Cas9 模块,成功把大肠杆菌获取耐药质粒的效率压低一到三十倍,为“基因层面”抗耐药开辟了新路径。本文用科普视角拆解这一思路、实验过程与应用前景。
一、CRISPR‑Cas:把“自卫系统”反向用作“封锁系统”
天然的 CRISPR‑Cas 是细菌对抗噬菌体的免疫武器:遇到入侵 DNA,细菌会把片段插进自身 CRISPR 阵列,当“记忆条形码”。下次再遭遇相同序列,Cas9 在向导 RNA(gRNA)的指引下精准切断外源 DNA。
科学家将这一逻辑反向利用:如果我们把 gRNA 代码写成“耐药基因序列”,当质粒通过转化、转导或接合进入宿主,Cas9 便会识别并剪断,阻止其在细胞中稳定复制。这样,细菌就像装上了“择友系统”,只要对方带着耐药“证件”,立刻拒之门外。
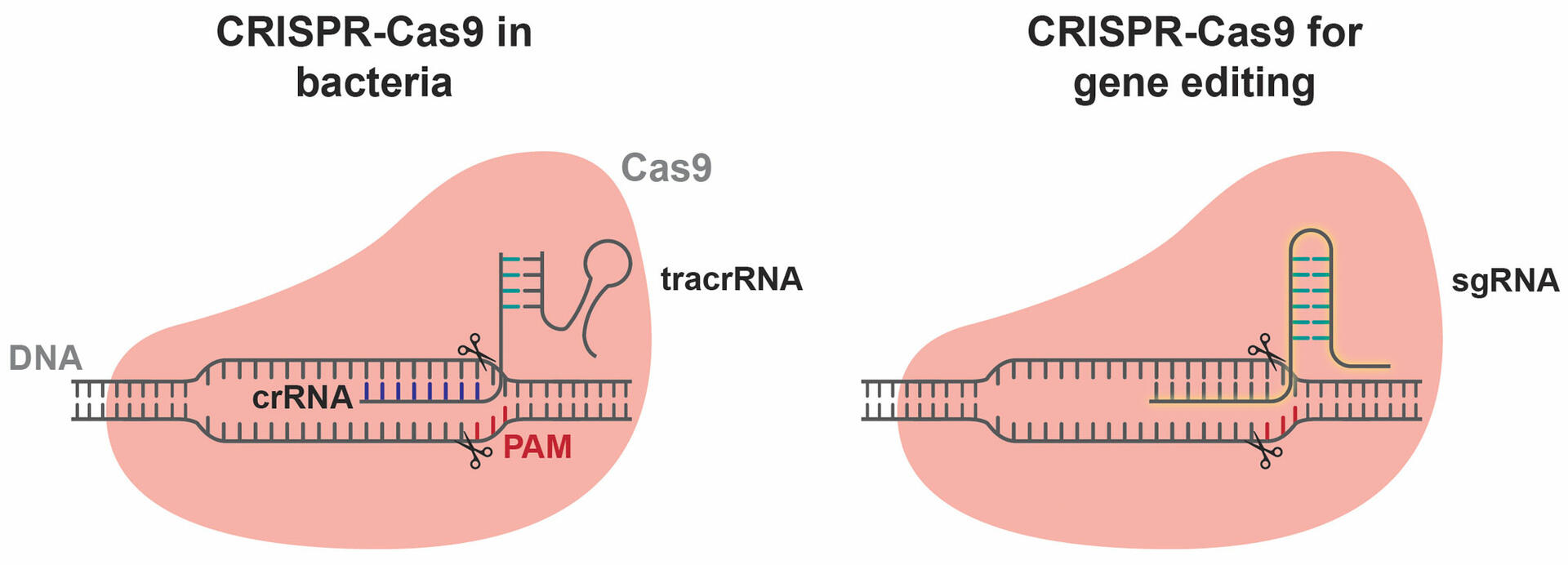
二、靶点设计:一张网兜住多种耐药基因
研究团队首先在 NCBI 抗性基因数据库中检索临床常见的 β‑内酰胺酶、氨基糖苷酶和四环素、氯霉素耐药基因序列,从中筛出保守区,最终确定 8 条 20 bp 靶序列。每条序列前紧跟 NGG PAM 以保证 SpCas9 识别。
随后把 8 条 crRNA 串联进单质粒,并配以 tracrRNA 与 cas9 组成全套表达盒。这样一张网覆盖了 blaTEM、blaCTX‑M、aadA、tetA、cat 等多种耐药因子,只要质粒带有其中任何一段,就难逃 Cas9 斩击。
三、实验路径:三种 HGT 途径逐个击破
- **化学转化**:将含耐药基因的质粒直接转入易感大肠杆菌。结果显示,CRISPR 组转化效率下降 10¹–10³ 倍,大部分菌落无法在含药平板上生长。
- **噬菌体转导**:利用 P1 噬菌体包装耐药片段,在无防护菌株中轻松感染,而带 Cas9 系统的菌株感染率骤降两个数量级。
- **接合转移**:将耐药质粒置于供体菌,通过性菌毛接合传递给受体菌。CRISPR 受体菌的接合成功率仅 0.03%,对比空载对照的 3% 显著降低。
四、数据解读:不仅“剪掉”,还“扼杀”
研究者进一步用实时 PCR 追踪质粒拷贝数,发现即便少数细胞侥幸获得耐药质粒,Cas9 会触发双链断裂,导致质粒不断降解并激活 SOS 反应,菌株生长速度显著下降。和单纯依赖抗生素压力不同,这种基因层扑杀不给耐药质粒任何演化空间。
五、“益生菌哨兵”与“环境防火墙”
◇ **肠道微生态守门员**:把 CRISPR‑Cas 抗耐药模块装进无害益生大肠杆菌,口服后在肠道建库,实时切断潜在耐药质粒的传播链。
◇ **污水处理屏障**:在生物膜或活性污泥中引入 CRISPR 抑制菌,减少医院排污中耐药基因向环境扩散。试验显示 12 小时可把 blaTEM 检出率压到 5%。
◇ **病原菌生物控制**:在养殖水体释放工程噬菌体,携带 cas9 mRNA + gRNA,专割耐药片段,降低多重耐药弧菌的爆发概率。
六、现实挑战:精准“剪刀”仍需安全“保护套”
- **靶序列变异**:质粒快速突变可能逃脱识别,需多靶 crRNA 或依赖 AI 预测热区。
- **离靶风险**:crRNA 与宿主基因高同源度时可能误剪,必须引入精准算法筛查脱靶位点。
- **水平扩散**:携带 cas9 的质粒自身也可能被转移,引发生态担忧,可通过自杀开关或抑制性复制元件限制。
- **免疫排斥**:部分细菌对外源 Cas9 有限制性修饰‑甲基化防御,需要选用菌源 Cas 或 Cas12f 微型核酸酶降低识别。
七、未来方向:从“封锁”到“过滤”
► **CRISPRi 阻断复制**:使用 dCas9 占位锁定 oriT 或 repA,而非切断 DNA,降低 SOS 应激。
► **可编程毒素‑抗毒素**:Cas9 精准插入自杀基因,仅在携带耐药序列时表达毒素。
► **群体感应触发**:将 CRISPR 模块置于 quorum‑sensing 控制下,只有细菌密度攀升才启动,减少能量负担。
► **机器学习抗性图谱**:结合全球污水宏基因组数据库,预测新兴耐药基因热区,实时更新 gRNA 库。
【小结】
CRISPR‑Cas 不再只是修基因的“手术刀”,也能成为阻断耐药传播的“海关剪”。这项研究用八把 gRNA 锁紧了常见耐药基因的“入境通道”,把转化、转导、接合三座桥梁同时拆除,为抗生素后时代提供了新的干预层级。当然,精准、可控、生态安全仍是下一阶段的关键词。真正在医院、农田、污水厂落地前,我们需要更智慧的算法、更严谨的生物安全框架,以及跨学科的监管共识。未来,当 CRISPR‑Cas 与益生菌、噬菌体、纳米载体联手,也许能把耐药危机的曲线拐向下坡路——这一天值得我们期待。
