外泌体提取6大方法全解析:原理、流程与优劣势对比
外泌体提取是研究的基础,不同方法的原理、效率和适用场景差异显著。本文系统梳理 超速离心法、试剂盒沉淀法、密度梯度离心法、超滤法、磁珠免疫法和尺寸排阻色谱法的实验原理、操作流程,并通过 8项关键指标横向对比,帮你快速选择最适合的提取方案。
一、超速离心法(差速离心):外泌体提取“金标准”
【实验原理】
基于颗粒沉降速度差异,通过逐步增加离心力(从低到高),依次去除细胞、碎片、微囊泡,最终在100,000g超速离心力下沉淀外泌体(外泌体沉降系数1.13-1.21g/mL)。
【核心流程】
以细胞上清为例
- 预处理:300×g(10min)→ 2,000×g(20min)→ 10,000×g(30min),去除细胞和碎片;
- 超速离心:100,000×g(70min,4℃)沉淀外泌体,PBS洗涤后再次100,000×g(70min)纯化;
- 收集:沉淀用PBS重悬,-80℃保存。
优劣势

二、聚合物沉淀法(试剂盒法):快速提取“新手首选”
【实验原理】
通过 PEG(聚乙二醇)等聚合物 竞争性结合水分子,降低外泌体溶解度,使其在低速离心(1,500-3,000×g)下与聚合物共沉淀(PEG分子量6000-8000效果最佳)。
【核心流程】
以ExoQuick试剂盒为例
- 预处理:样本3,000×g(15min)去除碎片;
- 沉淀:按1:5比例混合样本与沉淀试剂,4℃孵育12h(或30min快速沉淀);
- 离心:1,500×g(30min)收集沉淀,PBS洗涤去除残留PEG。
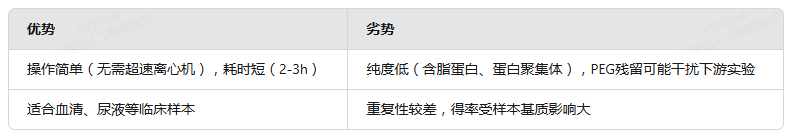
优劣势
三、密度梯度离心法:高纯度外泌体“进阶选择”
【实验原理】
在蔗糖/碘克沙醇密度梯度中,外泌体因密度(1.13-1.19g/mL)富集于特定梯度层,通过超速离心实现与杂蛋白、凋亡小体的分离。
【核心流程】
蔗糖密度梯度法
- 制备梯度:依次叠加60%、50%、40%、30%蔗糖溶液,形成连续密度梯度;
- 上样离心:样本加于梯度顶层,100,000×g(16h,4℃);
- 收集:取1.13-1.19g/mL密度层,PBS洗涤后离心沉淀。
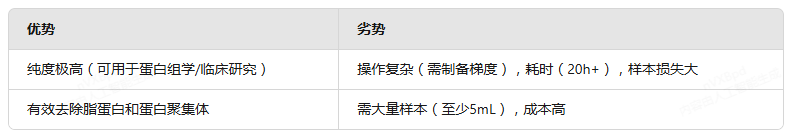
优劣势
四、超滤法:快速浓缩“小体积样本首选”
【实验原理】
利用 100kD截留分子量超滤膜,通过离心力截留外泌体(粒径>膜孔径),同时去除小分子杂质(蛋白、盐),实现浓缩与分离。
【核心流程】
- 超滤浓缩:样本加入100kD超滤管,4,000×g(30min)浓缩至0.5mL;
- 洗涤:加PBS重复超滤2次,去除残留杂质;
- 收集:倒转超滤管离心,收集截留液(外泌体)。
优劣势

五、磁珠免疫捕获法:特异性提取“靶向研究首选”
【实验原理】
磁珠表面包被外泌体特异性抗体(如抗CD63、CD9),通过抗原-抗体结合捕获目标外泌体,磁场分离后洗脱获得高特异性外泌体。
【核心流程】
- 孵育:磁珠与样本4℃孵育1h(抗体与外泌体结合);
- 分离:磁场吸附磁珠,PBS洗涤3次去除未结合杂质;
- 洗脱:用酸性缓冲液(pH 2.0)洗脱外泌体,中和后收集。
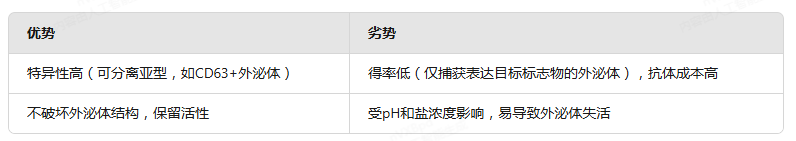
优劣势
六、尺寸排阻色谱法(SEC):临床样本“高活性首选”
【实验原理】
基于颗粒粒径差异,样本流经SEC色谱柱时,大粒径外泌体无法进入填料孔隙,先被洗脱;小分子杂质(蛋白、盐)进入孔隙,后被洗脱,从而分离纯化。
【核心流程】
以qEV柱为例
- 上样:样本经0.22μm过滤后上样(0.5mL/柱);
- 洗脱:用PBS洗脱,收集第9-10个组分(外泌体富集峰);
- 浓缩:洗脱液超滤浓缩至所需体积。
优劣势
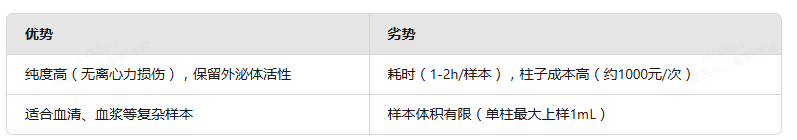
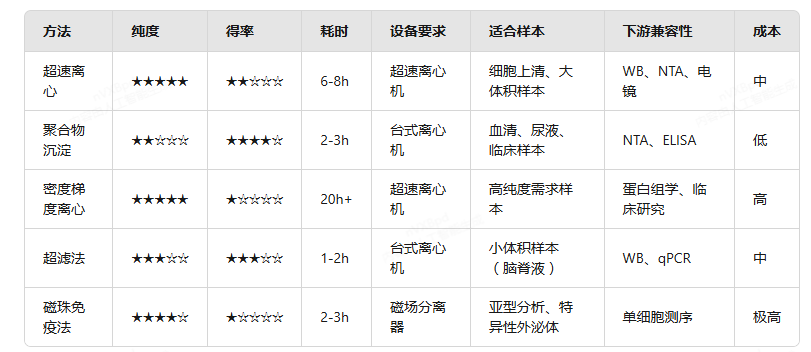
6大方法横向对比:8项指标帮你选