登刊Cell!脑内给药新路径:颅骨骨髓免疫细胞载药
 2026年1月17日,首都医科大学附属北京天坛医院神经病学中心、国家神经疾病医学中心王伊龙教授团队,携手清华大学张明君教授团队,于国际顶刊Cell在线刊发题为“Nanoparticles hijack calvarial immune cells for CNS drug delivery and stroke therapy”的研究成果。
2026年1月17日,首都医科大学附属北京天坛医院神经病学中心、国家神经疾病医学中心王伊龙教授团队,携手清华大学张明君教授团队,于国际顶刊Cell在线刊发题为“Nanoparticles hijack calvarial immune cells for CNS drug delivery and stroke therapy”的研究成果。
此项研究证实,经颅骨内注射白蛋白纳米颗粒,能够高效“劫持”颅骨髓系免疫细胞;这类载药细胞可规避血脑屏障(BBB),经由颅骨骨髓-硬脑膜-类淋巴系统的通路快速迁移至中枢神经系统病灶,将药物精准递送至受损神经元,最终达成急性与长期双重神经保护的成效。
BBB是中枢神经系统药物研发的核心瓶颈,现有治疗方案多依靠直接穿透血脑屏障,却普遍存在安全性风险与递送效率偏低的弊端。
此前,王伊龙教授团队曾发现,可依托颅骨骨髓与硬脑膜之间的天然微通路实现药物递送入脑,率先提出经颅骨骨髓-硬脑膜-类淋巴系统绕行血脑屏障给药的全新理论,并构建出适用于动物与人体的核心技术体系(相关成果发表于EbioMedicine 2025)。但药物靶向特异性不足的短板,往往会引发不良反应;加之多数神经疾病存在区域特异性易感特征,这类不良反应的解决难度更为棘手。
为此,王伊龙教授团队联合清华大学张明君教授团队,借鉴微纳机器人的设计理念,通过颅骨骨髓微创注射的方式,将白蛋白纳米颗粒直接输送至颅骨骨髓腔内。实验结果表明,这类纳米颗粒可被颅骨骨髓免疫细胞高效吞噬摄取,形成兼具靶向性与运载功能的“颅骨免疫细胞微纳机器人”,并沿前颅骨-脑膜微通路向中枢神经系统定向迁移。在啮齿类动物脑卒中模型中,该类“微纳机器人”的迁移能力显著提升,且在脑膜及脑卒中病灶区域高度富集。值得关注的是,当给药剂量仅为传统静脉注射方案的1/15时,经颅骨骨髓途径给予的脑细胞保护剂,仍能有效缩小脑梗死病灶体积、减轻脑水肿症状,显著改善实验动物的神经功能,且呈现出长达28天的长期预后优化效果。此外,团队还开展了经颅骨骨髓-硬脑膜-胶质淋巴系统给药技术首次人体探索性临床研究(SOLUTION试验),共纳入20例恶性大脑中动脉梗死患者。研究结果提示,该给药技术的手术耐受性佳且安全性表现优异,患者神经功能恢复进程展现出积极向好的趋势,为这一创新策略的临床转化奠定了初步基础。
该研究阐明并验证了基于颅骨骨髓-脑膜微通路与免疫细胞“载药”的全新递药机制,不仅为基于颅骨骨髓-硬脑膜-胶质淋巴系统的中枢神经系统疾病治疗提供了创新工具,更拓展了中枢神经系统精准给药的基础理论体系与技术支撑平台。这种经颅骨给药的创新策略具备普适性与可拓展性,为中枢神经系统疾病的治疗探索与机制研究提供了全新范式。
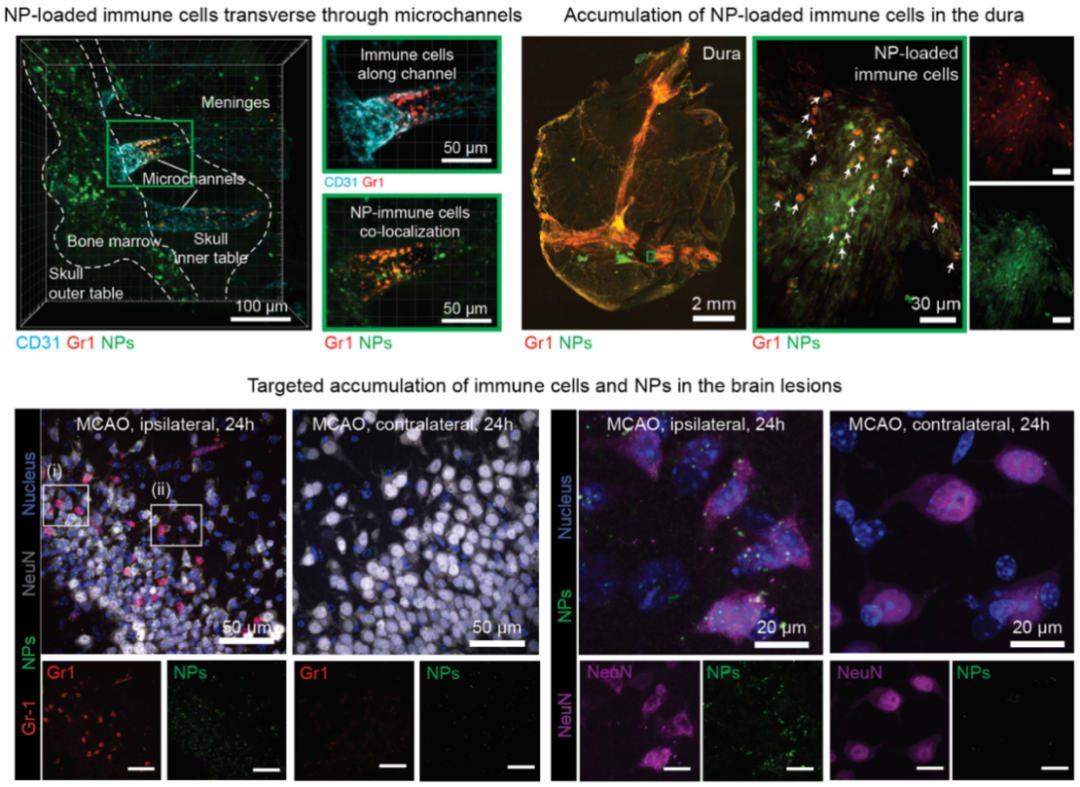
图 1 颅骨骨髓免疫细胞递送纳米颗粒至脑实质病灶
