流式实验全攻略:从样本制备到数据解读,新手也能少走弯路
在细胞生物学研究领域,流式细胞术绝对是“全能选手”——既能精准计数细胞,又能分析细胞表面标志物,还能分选特定细胞亚群,从基础科研的细胞表型分析到临床的肿瘤诊断,都有它的用武之地。但对流式新手而言,“样本处理不当导致数据紊乱”“荧光补偿没调好出现假阳性”等问题常常让人头疼。今天,我们就把流式实验的核心逻辑、操作关键和避坑技巧讲清楚,帮你轻松搞定这项实验技术。
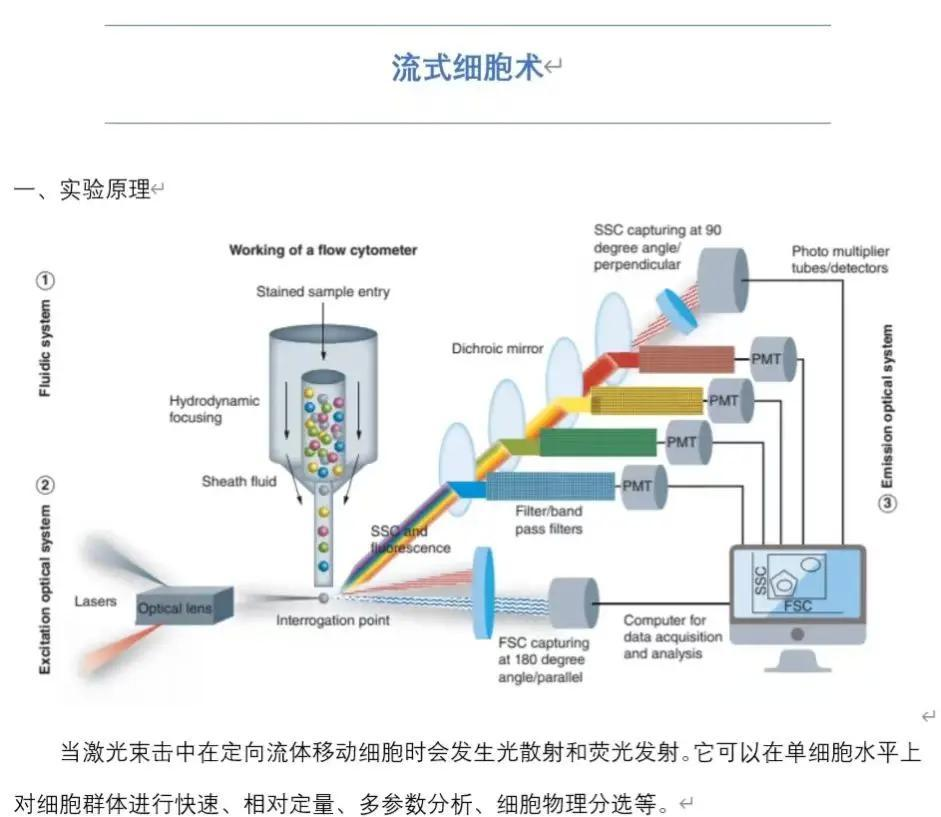
想要做好流式实验,先得摸清它的“工作套路”。流式细胞术的核心原理,是让单个细胞携带荧光信号,在液体流的带动下依次通过激光检测区域,激光照射到细胞上的荧光物质后产生散射光和荧光信号,这些信号被探测器捕捉并转化为数字信号,最终通过软件分析得到细胞的数量、表型等信息。简单来说,就像给细胞“贴标签”(荧光抗体),再让它们“逐个过安检”(激光检测),通过“标签信号”区分不同细胞类型,整个过程精准到单个细胞级别。
流式实验的核心价值在于“精准识别”与“高效分选”,但这一切都建立在规范操作的基础上。实验流程主要分为样本制备、抗体染色、仪器检测和数据解读四大环节,其中样本制备是“第一道关卡”,直接决定实验成败。不同类型的样本处理方式差异很大,这也是新手最容易出错的地方,我们先重点说说常见样本的处理技巧。
外周血样本是最常用的类型,处理核心是去除红细胞干扰。首先用EDTA抗凝管采集血液,避免凝血导致细胞聚集;然后按照1:1比例加入红细胞裂解液,室温避光孵育5-10分钟,裂解过程中要注意观察,避免裂解过度损伤白细胞;裂解完成后离心弃上清,用PBS缓冲液洗涤2次,最后调整细胞浓度至1×10⁶-1×10⁷个/mL,确保细胞分散均匀无沉淀。如果是小鼠脾脏等组织样本,需要先将组织剪碎,用研磨棒在筛网上轻轻研磨,获得单细胞悬液后再进行红细胞裂解,研磨时力度要适中,防止细胞破裂。
贴壁细胞的处理关键是“温和消化”,避免细胞表面标志物被破坏。先用PBS洗去培养基,加入0.25%胰酶-EDTA消化液,37℃孵育2-3分钟,在显微镜下观察到细胞变圆、间隙增大时立即终止消化;终止液推荐使用含10%胎牛血清的培养基,既能中和胰酶活性,又能保护细胞表面蛋白;随后轻轻吹打细胞获得单细胞悬液,离心洗涤后调整细胞浓度,吹打时动作要轻柔,避免产生过多气泡损伤细胞。
抗体染色是流式实验的“灵魂步骤”,特异性结合直接影响信号准确性。染色前要做好抗体选择,根据目标标志物选择对应的荧光抗体,同时注意抗体的克隆号和荧光素类型,避免荧光信号重叠;比如检测CD4和CD8时,可选择FITC标记的CD4抗体和PE标记的CD8抗体,两者荧光光谱重叠少,信号干扰小。抗体浓度也需严格控制,过高会导致非特异性结合,过低则信号微弱,建议按照抗体说明书的推荐浓度进行预实验,确定最佳染色浓度。
染色操作有明确的规范流程:先取100μL调整好浓度的细胞悬液加入流式管,加入适量抗体后轻轻混匀,4℃避光孵育20-30分钟,孵育过程中每隔10分钟轻轻颠倒流式管一次,确保抗体与细胞充分结合;孵育结束后加入2mL PBS,300g离心5分钟弃上清,重复洗涤2次,去除未结合的游离抗体;最后加入500μL PBS重悬细胞,待检测。如果进行胞内染色,还需要在抗体染色前进行细胞固定和通透处理,常用的固定剂是4%多聚甲醛,通透剂则根据抗体靶点选择 Triton X-100或皂素。
仪器操作与参数设置是“精准捕获信号”的关键。上样前要检查流式细胞仪的状态,确保激光强度稳定、液流顺畅,先用标准微球进行仪器校准,调整前向散射光(FSC)、侧向散射光(SSC)的电压,使细胞群体清晰分离。上样时要控制好流速,低速上样(约1000个细胞/秒)能减少细胞重叠,提高数据准确性;如果样本细胞浓度过低,可适当提高流速,但需避免超过3000个细胞/秒。检测过程中要密切观察散点图,若出现细胞聚集明显的情况,应立即停止上样,将样本重新吹打混匀后再检测。
荧光补偿调节是避免信号干扰的“核心技巧”,也是新手的难点。由于不同荧光素的发射光谱存在重叠,比如PE的荧光信号可能会干扰APC通道,导致假阳性结果。调节补偿时,需设置单阳性对照管和空白对照管,以空白对照为基准,通过软件调整各通道的补偿值,使单阳性细胞在其他荧光通道的信号回归到阴性水平。建议每次实验前都重新调节补偿,尤其是更换抗体批次或仪器时,不能直接沿用之前的补偿参数。
数据解读要遵循“先质控后分析”的原则。首先查看细胞存活率,通过7-AAD或PI染色排除死细胞,死细胞会释放非特异性荧光,导致结果偏差,通常要求活细胞比例在90%以上;然后观察细胞群体的分群情况,通过FSC和SSC散点图圈定目标细胞群体,排除细胞碎片和聚集物;最后分析目标标志物的表达情况,通过门控策略准确圈定阳性细胞,计算阳性率和平均荧光强度。数据解读时要结合对照实验,空白对照排除自发荧光,同型对照排除非特异性结合,只有这样才能得到可靠的结果。
新手常踩的“坑”有哪些?不少人样本处理时离心速度过高(超过500g),导致细胞破裂;抗体染色时在室温下进行,容易引发非特异性结合;上样前忘记过滤样本,细胞聚集堵塞仪器喷嘴;还有人解读数据时不设对照,直接判定阳性结果,这些操作都会严重影响实验质量。另外,流式管的选择也不能忽视,要使用专用的聚苯乙烯流式管,避免使用玻璃管或普通离心管,防止细胞吸附影响计数。
流式实验的精髓在于“细节决定成败”,从样本的每一次离心、抗体的每一滴加入,到仪器的每一次校准,都需要严谨细致。新手不必因复杂的步骤而退缩,只要掌握样本处理的核心技巧,做好对照实验,熟练运用仪器和分析软件,就能逐步提升实验水平。你在流式实验中遇到过哪些难题?欢迎在评论区留言分享,我们一起交流解决,让每一次实验都能精准高效!
图片来源于百度
