细胞实验实操指南:从培养到检测,三大核心环节
细胞实验是基础医学研究的核心手段,从细胞培养、转染到检测分析,每个环节的操作细节都直接影响实验结果的可靠性。新手常因忽视无菌操作、参数设置不当等问题导致实验失败,资深研究者也可能因流程不规范出现数据偏差。本文聚焦细胞实验最关键的三大环节,拆解标准化操作方法和高频注意事项,帮你少走弯路、提高实验成功率。
核心环节一:细胞培养 —— 无菌操作与状态维持
细胞培养的核心目标是维持细胞的正常生理状态,避免污染和异常增殖,这是后续所有实验的基础。首先,无菌环境构建是重中之重:实验前需用 75% 酒精擦拭超净工作台台面、器械及操作者双手,紫外线照射工作台 30 分钟后通风 15 分钟,避免紫外线残留损伤细胞。所有操作需在工作台内进行,瓶口开启后始终朝向酒精灯火焰,吸管、移液枪头避免接触非无菌区域,实验结束后及时清理台面并再次消毒。
细胞复苏与传代的操作细节直接影响细胞活性:复苏时需将冻存管快速放入 37℃水浴锅,不断摇晃至冰块完全融化(全程不超过 1 分钟),避免低温损伤细胞;离心后弃去冻存液,用预热的完全培养基重悬细胞,接种密度需根据细胞类型调整(贴壁细胞通常为 5×10⁴~1×10⁵ cells/cm²),接种后轻轻摇晃培养瓶使细胞均匀分布。传代时需控制胰酶消化时间,待细胞边缘收缩、间隙增大时立即加入完全培养基终止消化,吹打细胞时动作轻柔,避免产生过多气泡损伤细胞膜,传代比例一般为 1:2~1:4,过快传代易导致细胞生长缓慢,过密则可能引发接触抑制。
细胞培养过程中需定期观察状态:每天通过显微镜观察细胞形态(贴壁细胞是否舒展、悬浮细胞是否均匀)、密度和有无污染,若发现培养基浑浊、出现异常颗粒或菌丝,需立即丢弃污染细胞,避免扩散。同时,培养基需根据细胞类型选择合适的血清浓度(通常为 10%~20%),并定期更换(贴壁细胞每 2~3 天更换一次,悬浮细胞每 1~2 天更换),维持 pH 值稳定(7.2~7.4),培养箱温度、湿度和 CO₂浓度(5%)需严格控制,避免波动影响细胞生长。
核心环节二:细胞转染 —— 参数优化与效率验证
细胞转染是将外源基因导入细胞的关键技术,常用方法包括脂质体转染、病毒转染和电穿孔转染,不同方法的操作要点和适用场景差异显著。脂质体转染操作简便、毒性较低,适用于大多数贴壁细胞和悬浮细胞:转染前需将细胞接种至 6 孔板,待汇合度达到 70%~80% 时进行转染,脂质体与质粒的比例需根据细胞类型优化(通常为 2:1~3:1),混合后室温孵育 20 分钟形成复合物,滴加至细胞培养基中时轻轻摇晃,转染后 6~8 小时更换新鲜培养基,避免脂质体毒性影响细胞活性。
病毒转染效率高、适用于难转染细胞,但需注意生物安全和病毒滴度:使用慢病毒、腺病毒等载体时,需在生物安全二级实验室操作,佩戴手套、口罩等防护装备;转染前需测定病毒滴度,根据细胞类型调整感染复数(MOI 值),通常为 10~50,感染时可加入聚凝胺(Polybrene)提高病毒吸附效率,但需提前通过预实验确定安全浓度,避免细胞毒性。电穿孔转染适用于原代细胞等难转染细胞,关键是优化电压、电容和脉冲时间,过高电压会导致细胞死亡,过低则转染效率低下,转染后需立即加入预热的培养基,帮助细胞恢复活性。
转染效率验证是不可或缺的步骤:转染后 24~48 小时,可通过荧光显微镜观察报告基因(如 GFP)的表达情况,初步判断转染效率;若需精准定量,可采用流式细胞术检测荧光阳性细胞比例,或通过 qPCR、Western blot 检测目的基因的 mRNA 和蛋白表达水平。若转染效率过低,需排查细胞状态、质粒质量、转染试剂比例等因素,必要时更换转染方法或优化参数。
核心环节三:细胞检测 —— 样本处理与数据解读
细胞实验的检测方法需根据研究目的选择,常见包括细胞增殖检测(CCK-8、MTT)、凋亡检测(流式细胞术、TUNEL)、蛋白表达检测(Western blot)等,每个检测方法的样本处理和操作细节都需严格遵循标准流程。以 CCK-8 检测为例:检测前需将细胞接种至 96 孔板,每组设置 3~5 个复孔,避免单次实验误差;加入 CCK-8 试剂后,需在 37℃孵育 1~4 小时,根据细胞增殖情况调整孵育时间,吸光度检测时需在 450nm 波长下进行,同时设置空白对照孔(仅含培养基和 CCK-8 试剂),扣除背景值后计算细胞增殖率。
Western blot 检测的关键在于样本制备和蛋白分离:细胞裂解时需加入蛋白酶抑制剂和磷酸酶抑制剂,防止蛋白降解和去磷酸化;蛋白定量需采用 BCA 法或 Bradford 法,确保上样量准确(通常为 20~50μg);SDS-PAGE 电泳时,分离胶浓度需根据目的蛋白分子量调整(小分子蛋白用 12%~15% 凝胶,大分子蛋白用 8%~10% 凝胶),转膜时需注意膜的类型(PVDF 膜适用于大多数蛋白,硝酸纤维素膜适用于小分子蛋白)和转膜电流、时间,避免转膜不完全或过度。孵育一抗和二抗时,需控制抗体浓度和孵育时间(4℃过夜孵育一抗,室温孵育二抗 1~2 小时),洗膜步骤需充分,避免非特异性结合导致的条带杂带。
数据解读时需注意实验重复性和统计学分析:每个实验至少独立重复 3 次,数据以 “均值 ± 标准差(mean±SD)” 表示,采用 SPSS 或 GraphPad Prism 软件进行统计学分析,组间比较采用 t 检验或方差分析,P<0.05 视为差异具有统计学意义。同时,需结合实验目的解读数据,避免过度解读或误读结果,例如细胞增殖率升高不一定代表细胞活性增强,需结合细胞形态、凋亡率等指标综合判断。
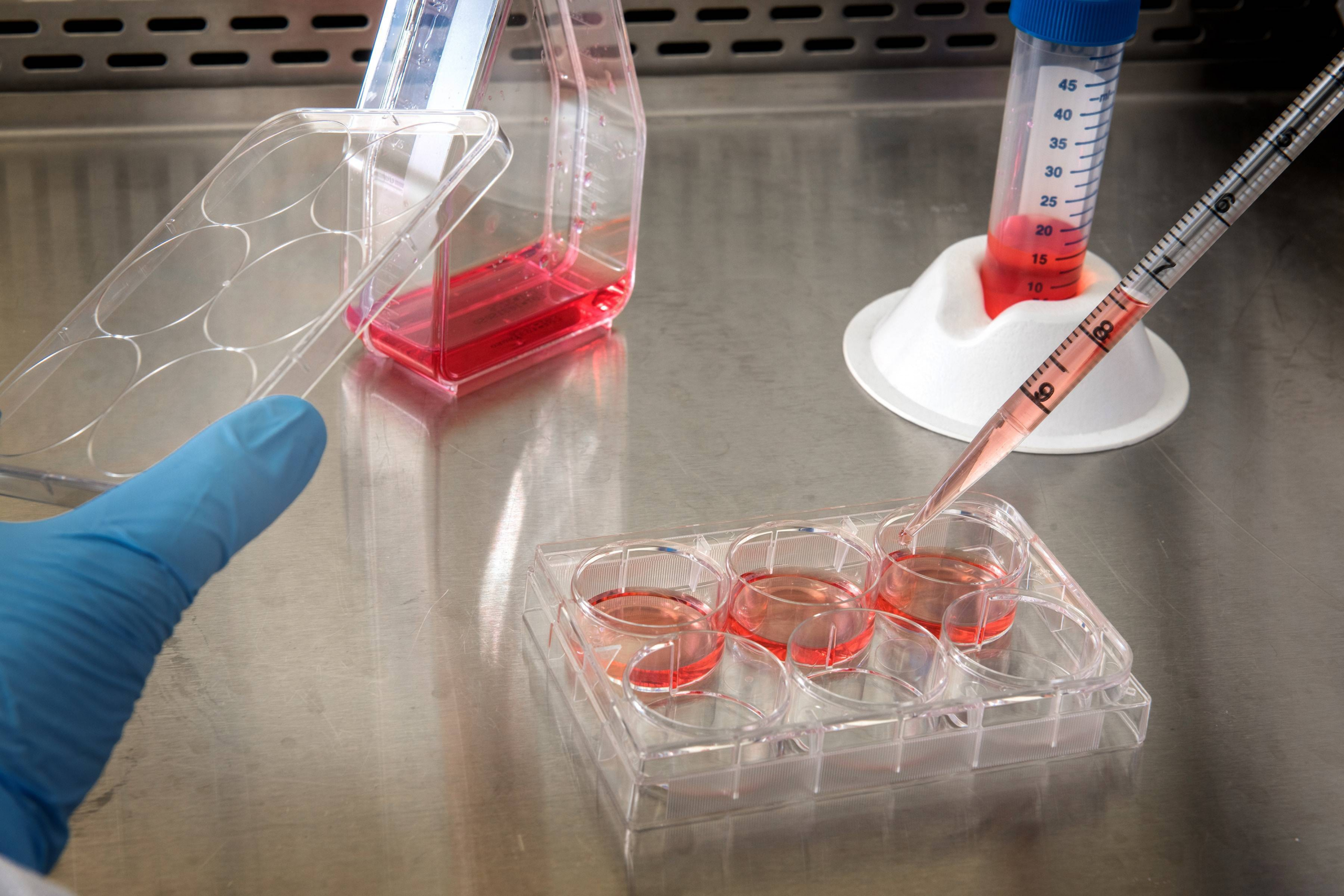 图片来自百度图库
图片来自百度图库
