揭秘去泛素化:细胞内的“蛋白命运改写师”,藏着疾病治疗的新密码
在人体细胞这个精密的“生命工厂”里,每一种蛋白质都有明确的“生命周期”——从合成、发挥功能到最终降解,全程受严格调控。其中,“泛素化”就像给待降解蛋白贴上“回收标签”,指引它们进入蛋白酶体被分解,维持细胞内环境的有序运转。
但你知道吗?细胞内还存在一套“反向操作”机制——去泛素化。它如同一位精准的“标签剥离工”,能移除蛋白上的泛素标签,逆转其降解命运,甚至改写蛋白的功能走向。这个看似简单的“可逆过程”,实则是调控细胞生理活动的核心枢纽,更成为近年来肿瘤、神经退行性疾病等难治性疾病的研究热点。今天,我们就来深入解锁去泛素化的神秘世界。
一、基础认知:去泛素化是什么?—— 泛素系统的“平衡调节器”
要理解去泛素化,首先得搞懂它的“搭档”——泛素化。泛素是一种由76个氨基酸组成的高度保守蛋白,几乎存在于所有真核生物中,就像细胞内的“通用标签”。
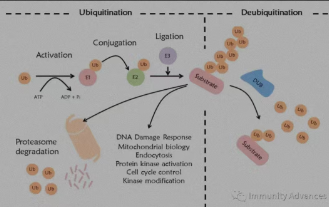
泛素化过程需要E1激活酶、E2结合酶、E3连接酶三步级联反应,将泛素分子以共价键形式连接到目标蛋白上。根据泛素连接位点(7个赖氨酸残基)的不同,会形成结构多样的多聚泛素链,其中最常见的K48型泛素链会启动蛋白降解,而K63型则参与信号传导、DNA损伤修复等过程。
而去泛素化,就是由去泛素化酶(DUBs)介导的逆反应,通过切割泛素与蛋白之间、或泛素与泛素之间的共价键,实现三大核心功能:一是释放游离泛素分子,循环再利用;二是修剪泛素链,改变其结构和功能;三是彻底移除泛素标签,保护蛋白不被降解,恢复其活性与功能。
如果把泛素化比作“给蛋白判死刑”,去泛素化就像是“死刑复核与赦免”,两者共同构成泛素系统的动态平衡。这种平衡是维持蛋白稳态、细胞正常生理功能的基石,一旦失衡,就可能引发一系列疾病。
二、核心执行者:去泛素化酶(DUBs)的“家族图谱”
去泛素化的精准执行,完全依赖于去泛素化酶(DUBs)的特异性作用。目前已知人类细胞中约有86种DUBs,根据结构和作用机制的不同,可分为7个家族,各自承担不同的“职责”:
- 泛素特异性蛋白酶(USPs):家族成员最多(58个),功能最多样化,多数为“杂食性”酶,能识别多种泛素链类型,参与细胞周期、免疫应答等多个过程,也是疾病研究中最受关注的家族。
- 泛素C末端水解酶(UCHs):主要作用于小分子泛素衍生物,参与神经元功能调控,其中UCH-L1的突变与帕金森病密切相关。
- 卵巢肿瘤蛋白酶(OTUs):具有明显的泛素链连接类型特异性,在炎症反应、病毒感染等过程中发挥关键作用。
- Machado-Joseph结构域蛋白酶(MJDs):与神经系统疾病相关,部分成员突变会导致脊髓小脑性共济失调。
- JAMM金属蛋白酶家族:唯一的金属依赖型DUBs,参与核糖体组装、细胞信号传导等过程。
- MINDY家族和ZUFSP家族:较新发现的家族,分别偏好切割K48型和线性泛素链,功能仍在深入探索中。
值得注意的是,约10%的DUBs属于“假酶”——虽无催化活性,但能通过参与蛋白复合物组装、调控其他酶活性发挥作用,丰富了去泛素化系统的调控网络。这些酶的活性受到磷酸化、乙酰化、蛋白相互作用等多重调控,确保其在正确的时间、位置发挥功能。
三、功能探秘:去泛素化如何调控细胞命运?—— 从生理到病理的关键枢纽
去泛素化酶通过精准调控蛋白的泛素化状态,深度参与几乎所有核心细胞过程,是细胞内的“多功能调控器”。
在正常生理过程中,去泛素化的核心作用包括:维持蛋白稳态,避免异常蛋白积累;调控DNA损伤修复,如USP1通过去泛素化稳定复制叉,修复DNA链损伤;参与免疫应答,调节NF-κB等炎症信号通路,平衡促炎与抗炎反应;维持线粒体功能,通过调控线粒体自噬,清除受损线粒体,保障细胞能量供应。
而当DUBs功能异常时,就会打破细胞平衡,诱发多种疾病。这也是去泛素化研究成为医学热点的核心原因:
- 肿瘤领域:DUBs既是“癌基因”也是“抑癌基因”
许多DUBs通过稳定癌蛋白或抑制抑癌蛋白降解,推动肿瘤发生发展。例如,USP7可去泛素化并稳定MDM2和p53,其中对MDM2的稳定会促进p53降解,导致癌细胞逃脱凋亡;USP28则直接稳定突变型p53,增强癌细胞侵袭能力,与膀胱癌进展密切相关。
同时,部分DUBs也发挥抑癌作用,如USP15通过去泛素化PTEN,增强其抑癌活性。这种“双向调控”特性,让DUBs成为肿瘤靶向治疗的潜力靶点——通过抑制致癌DUBs或激活抑癌DUBs,实现肿瘤干预。
- 神经退行性疾病:DUBs是“蛋白清理工”的指挥官
阿尔茨海默病、帕金森病等疾病的核心病理特征,是异常蛋白(如β淀粉样蛋白、α-突触核蛋白)的聚集沉积。DUBs通过调控这些异常蛋白的降解,影响疾病进展。
例如,USP30的缺失可增强线粒体自噬,减少α-突触核蛋白积累,延缓帕金森病神经退化;而UCH-L1突变会导致其去泛素化活性下降,无法有效清除异常蛋白,加速神经元损伤。这为神经退行性疾病的治疗提供了新方向——通过调控DUBs活性,增强异常蛋白降解,缓解病理损伤。
- 其他疾病:从炎症到衰老的广泛参与
在炎症性疾病中,OTU家族成员可通过调控炎症信号通路,抑制过度炎症反应;在衰老相关疾病中,随着年龄增长,DUBs活性下降,导致泛素化蛋白积累,细胞功能衰退,成为老年痴呆、骨质疏松等疾病的重要诱因。
四、临床前景:DUBs靶向药物——难治性疾病的新希望
鉴于DUBs在疾病中的核心作用,靶向DUBs的药物开发已成为生物医药领域的热门方向。目前,主流策略是开发DUBs小分子抑制剂,部分药物已进入临床研究阶段,展现出良好的应用前景。
在肿瘤治疗中,USP1抑制剂可通过阻断DNA损伤修复,增强BRCA缺陷型肿瘤对化疗、放疗的敏感性,目前已进入临床Ⅰ期试验;P5091作为USP7/USP47双重抑制剂,能诱导多发性骨髓瘤、卵巢癌细胞凋亡,对耐药细胞也有效。在神经退行性疾病领域,USP30抑制剂MTX-325用于帕金森病的治疗已进入临床Ⅰ期,为这类无法治愈的疾病带来新曙光。
除了小分子抑制剂,泛素变体(UbVs)、基于活性的探针(ABPs)等新型工具也在快速发展。UbVs可特异性结合DUBs,阻断其与底物的相互作用,且能靶向小分子难以作用的蛋白界面;ABPs则可精准检测DUBs活性,为药物筛选和机制研究提供支撑。
不过,DUBs靶向药物开发仍面临诸多挑战:家族成员催化结构域高度保守,难以实现高特异性抑制;部分DUBs功能复杂,抑制后可能引发脱靶效应;药物递送效率不足,难以穿透血脑屏障等组织屏障。这些问题需要通过结构生物学、人工智能药物设计等多学科技术融合,逐步突破。
五、总结:去泛素化的未来——从机制研究到临床转化的黄金时代
从最初被视为泛素化的“附属过程”,到如今成为独立的研究热点,去泛素化的科学价值和临床潜力正被不断挖掘。它不仅揭示了细胞内蛋白调控的精妙网络,更为肿瘤、神经退行性疾病等难治性疾病提供了全新的治疗靶点。
随着冷冻电镜、单细胞测序、AI辅助药物设计等技术的应用,我们对DUBs的结构、功能及调控机制的理解将更加深入,有望突破现有研究瓶颈,开发出更多高特异性、低毒性的DUBs靶向药物。未来,去泛素化领域必将迎来从基础研究到临床转化的爆发式发展,为人类健康带来新的突破。
你还想了解去泛素化在某类疾病中的具体应用吗?欢迎在评论区留言,我们将持续为你解读前沿生物医学进展。